复宏汉霖:下一代TCE、ADC平台效果优异创新管线持续扩充
HLX43治疗复发或转移性食管鳞癌的二期临床数据,也表现优异。截至2025年11月25日,该二期临床共计入组37例患者,2mg/kg、2.5mg/kg、3.0mg/kg剂量组分别入组12例、12例、13例患者。86.5%的患者ECOG评分为1,既往接受治疗线,所有患者均接受过化疗及免疫治疗。疗效方面,33例患者可评估疗效,ORR为30.3%,DCR为81.8%。3mg/kg剂量组13例患者可评估疗效,ORR为61.5%,DCR为100%,其中10例PD-L1联合阳性分数(CPS)≥1的患者ORR为60.0%,DCR为100%。2例PD-L1联合阳性分数(CPS)<1的患者ORR为50.0%,DCR为100%。
除了PD-L1 ADC,从这次JPM上展示的早期管线来看,其核心竞争力正从单一产品转向系统的、平台化的创新布局,不局限于快速跟进(Fast-follow),更是在特定赛道打造“同类最优”甚至“同类首个”。最新管线不仅覆盖IO及ADC的升级版本,同时在TCE,ADC领域都有新的规划,并取得一定突破。
值得一提的是,复宏汉霖布局下一代TCECD3/CD28/TAA多特异性抗体平台,主要用于解决实体瘤免疫细胞浸入少的问题,开发安全的具有T细胞共刺激信号的TCE,更持久的激活和增殖T细胞,进而实现治疗窗口的改善。CD28双抗,三抗,行业内从未停止开发的脚步,尤其赛诺菲曾经开发多条CD3/CD28/TAA管线,其失败可以说是必然,其发表在《nature cancer》上的文章“Trispecific antibodies enhance the therapeutic efficacy of tumor-directed T cells through T cell receptor co-stimulation”中,数据表明仅有CD28抗体与CD3抗体在没有TAA靶向的情况下依然展现了非常高的杀伤能力,也就是说CD3和CD28的信号,不需要肿瘤相关抗原的特异性激活就会产生共刺激,虽然三抗具有更高的活性,但是这种机制的存在也是非常致命的,因为CD3和CD28是固有表达,具有广谱性,这种非靶向性激活增加了非靶点介导的毒性和CRS,从而大大降低给药剂量,使其无法奏效。
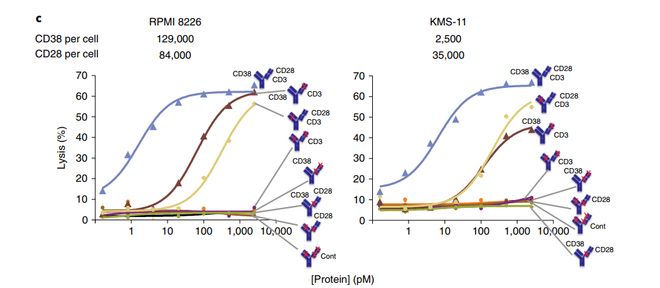
所以实现T细胞的靶点依赖性激活和CD3与CD28的cis-结合在改善治疗窗口中非常重要。根据复宏汉霖的数据显示,其CD3/CD28/TAA平台具有明显的TAA依赖活性,在没有TAA的情况下毫无活性。如下图所示。在没有Steap1的时候,毫无活性,三抗活性最高,CD3双抗次之,当CD28结合域被替代后该三抗几乎失去活性。CD28的激活依赖于CD3。这种设计最大程度上保有安全性窗口。
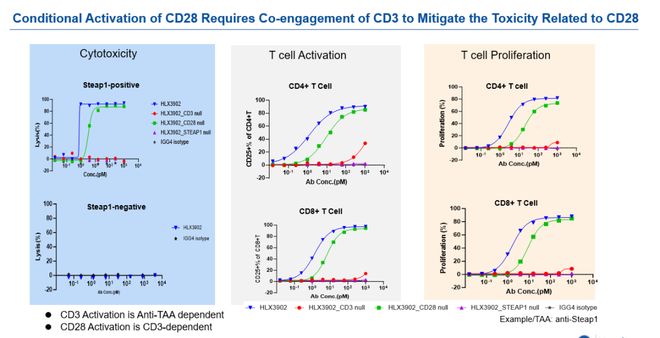
小细胞肺癌和前列腺癌多为免疫荒漠,具有共刺激信号的TCE在该类实体的应用空间更有利于改善肿瘤微环境。所以复宏汉霖开发了CD3/CD28/DLL3(HLX3901)和CD3/CD28/Steap1(HLX3902)。HLX3901,作为一款靶向DLL3(采用双表位设计)、CD3和CD28的四特异性TCE。其双表位设计可增强对肿瘤细胞的靶向性和特异性,而CD3/CD28信号的共激活则能增强T细胞的杀伤能力与持久性。与Tarlatamab相比,HLX3901展现出更优的细胞毒性效应,特别是在低效靶比条件下;在人类泛T细胞重构模型中,
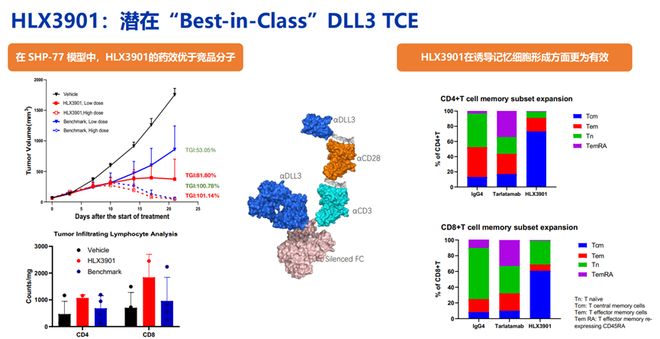
HLX3902 ,作为一款靶向CD3×CD28×STEAP1的三特异性TCE,能够将T细胞重定向至STEAP1阳性的前列腺肿瘤,并通过同时激活CD3与CD28信号增强T细胞功能。目前安进的CD3/Steap1展现了不错的临床药效。在临床前药效模型中,在低剂量组HLX3902展现了优异的抗肿瘤活性,具有更好的治疗窗口。同时,具有更多的T细胞浸润,且更加持久。
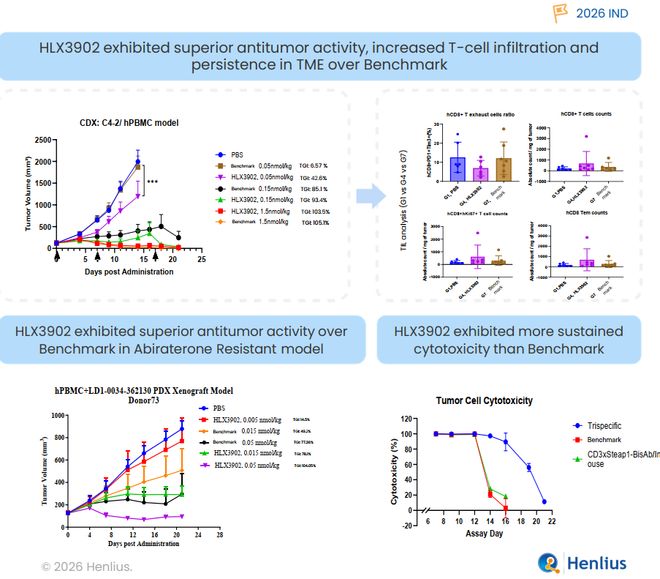
与此同时,复宏汉霖内研新一代ADC平台,采用了高亲水性的单元配件,同样选用GGFG作为linker,毒素方面采用更强旁观者效应的喜树碱payload。
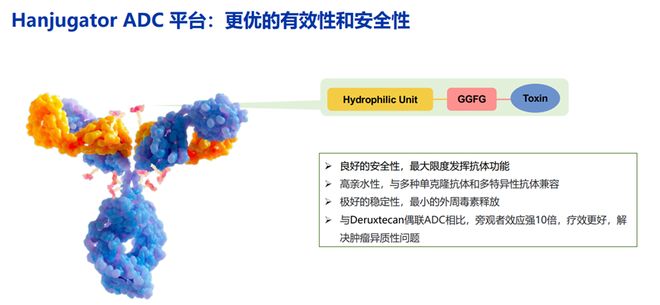
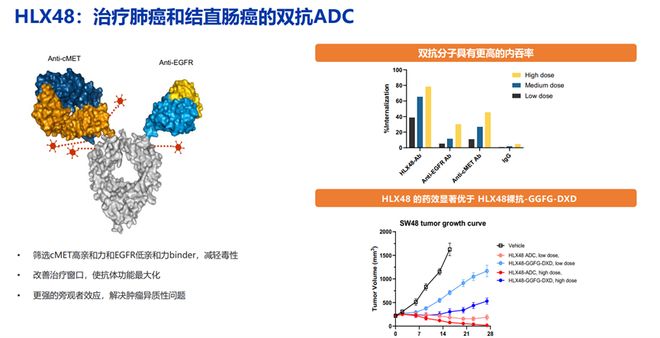
其中HLX48,EGFR/cMet双特异性ADC,便是采用上述ADC平台,潜在可用于NSCLC、CRC等实体瘤治疗,该靶点组合已知需要更高临床剂量才能实现最佳受体占据和疗效。尽管payload上和Exatecan等都属于TOPO1i类毒素,但较Exatecan等高活性载荷HLX48选择了中等活性载荷,有望将临床剂量提高,拓宽治疗窗,实现最佳受体占据和疗效。同时,研究显示,该偶联物旁观者杀伤效应较Deruxtecan强数倍以上。目前EGFR/cMet双抗在肺癌,结直肠等适应症都取得了很好的进展,其ADC在更高的治疗窗口的ADC平台有望能够起到双重作用。
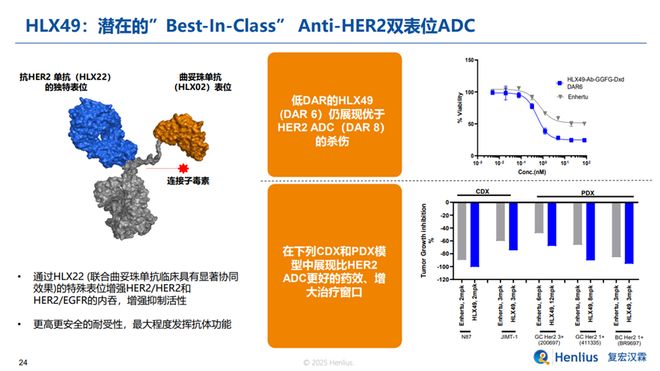
HLX49,作为一款靶向HER2双表位的ADC,潜在适应症为乳腺癌、胃癌等。该分子基于复宏汉霖HLX22与HLX02的结合表位特征开发,后者的联合方案在体内外均表现出优于HLX02(曲妥珠单抗)联合HLX11(帕妥珠单抗生物类似药)的抗肿瘤活性。临床前研究中,HLX49在多种CDX和PDX模型中 较Enhertu展现了更高的抗肿瘤活性。
潜在的大药方面,复宏汉霖基于新一代IO平台自研的PD-L1/VEGF双抗,项目编号HLX37,目前也已处于I期临床开发阶段。HLX37的作用机制结合了两种治疗路径:1)阻断PD-1 /PD-L1结合,2)阻断血管生成通路,双靶点设计有望产生协同抗肿瘤效应,并可能降低耐药性风险,通过特异性结合肿瘤细胞PD-L1实现肿瘤内部具有抗VEGF功能的HLX37 双抗分子的富集,实现大于抗PD-L1 单抗和抗VEGF 单抗的联合疗效。临床前研究表明,HLX37具有优异的抗肿瘤活性且安全性可控,同时能增强肿瘤富集效应,其在多类肿瘤中具有广泛的应用潜力。
KAT6A/B抑制剂HLX97,也展现出潜在的同类最佳的趋势,有望用于乳腺癌等实体瘤的治疗。根据在2025 AACR公布的临床前数据,与参比化合物PF-07248144相比,HLX97展现出更强的KAT6A/B抑制活性和对KAT5/7/8更高的选择性。同时,HLX97显示出良好的ADME特性,包括高口服生物利用度和优异的药代动力学特征。
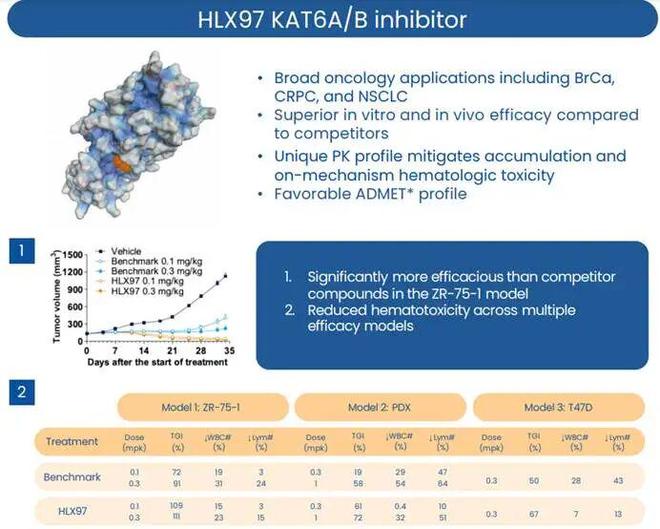
值得关注的是,在临床前研究中,HLX97在更低剂量下(约1/3)即展现出与参比化合物相当或更优的抗肿瘤活性。例如在ZR-75-1模型中,HLX97在0.1 mg/kg剂量下即可实现111%的肿瘤生长抑制率,而PF-07248144达到91%抑制率则需0.3 mg/kg的剂量(约为HLX97的3倍)。该趋势在PDX模型中亦得到验证。更关键的是,在达到相近抑瘤水平时,HLX97引发的血液学毒性显著更低。在ZR-75-1模型中,HLX97(0.1 mg/kg,TGI 111%)引起的白细胞下降比例仅为15%,而PF-07248144(0.3 mg/kg,TGI 91%)则导致31%的白细胞下降。在PDX模型中,这一差异更为显著:在相近疗效下,HLX97仅引起约0.4%的白细胞减少,而PF-07248144组则高达54%。对淋巴细胞的影响趋势和白细胞一致。以上数据表明,HLX97在临床前研究中展现出更优的效毒分离特性。在实现强效抗肿瘤活性的同时,其血液毒性——尤其是白细胞与淋巴细胞减少——显著低于同靶点参比化合物。鉴于剂量限制性血液毒性是该靶点药物开发的主要临床挑战,HLX97所展现出的这一差异化特征,可能源于其优化的药代动力学特性,使其在肿瘤组织与造血系统间具有更佳的选择性,从而预示其在临床上可能拥有更宽的治疗窗口。复宏汉霖以PDL1 ADC为切入口,逐步开始走往引领国内创新药发展的趋势。在此之前,可能对于PDL1 ADC,并没有人关注和在意,如今的优异疗效,跟随者不计其数。同时新一代TCE平台,正在逐步进入临床,无论是疗效上还是安全性上都表现出了优异的数据,未来更令人期待。



